К проводникам или
проводниковым материалам относятся материалы, хорошо проводящие электрический ток.
Обычно, это металлы, но также используются некоторые жидкости и ионизированные
газы.
По характеру
температурной зависимости проводимости проводники делятся на два типа:
проводники I рода и проводники II рода. У проводников I
рода проводимость с ростом температуры уменьшается. К проводникам I рода относятся металлы. У проводников II рода проводимость с ростом температуры увеличивается. К
проводникам II рода относятся
жидкости (электролиты), ионизированные газы.
Проводники,
применяемые в технике делятся на:
·
материалы
высокой проводимости (Ag, Cu, Al);
·
высоконагревостойкие
металлы (W, Mo, Ta, Nb,
Ti,
Zr,
Re);
·
металлы и
сплавы различного назначения (Ni, Hg);
·
щелочные
металлы (Li, K, Na, Cs, F);
·
щелочноземельные
металлы (Ca, Mg, Ba, Ra)
·
сплавы сопротивления;
·
контактные
материалы;
·
металлы и
сплавы электровакуумной техники (Pd);
·
припои и
флюсы;
·
электроугольные
изделия.
Качество
проводниковых материалов определяется электрическими, тепловыми и механическими
свойствами. Из электрических свойств основными считают удельную
электропроводность или обратную ей величину – удельное сопротивление r (Ом×м) и
температурный коэффициент удельного сопротивления ТКr.
Из тепловых свойств: теплопроводность, температурный коэффициент линейного
расширения.
3.1. Материалы
высокой проводимости
Материалы высокой проводимости применяются в качестве монтажных и
обмоточных проводов, соединительных, силовых и специальных высокочастотных
кабелей, проводящих элементов радиодеталей и узлов электронной аппаратуры. К
материалам высокой проводимости относятся медь и ее сплавы (бронза, латунь), алюминий и его сплавы (дюралюминий, альдрей), железо и стали, титан, никель, кобальт,
серебро, золото, платина, цинк, кадмий.
Медь
Широкое применение
меди обусловлено ее высокой электропроводностью, хорошей теплопроводностью,
химостойкостью, ковкостью, вязкостью, высокими механическими свойствами. Медь
часто встречается в самородном состоянии. Легко подвергается механической
обработке, т.к. обладает высокой пластичностью. Добывают медь из оксидных и
сульфидных руд. Их обжигают, плавят и получают черновую медь, которую
подвергают рафинированию электролитическим методом. Для этого из черновой меди
изготовляют аноды и проводят электролиз CuSO4.
Чистая медь, которая
применяется в электро- и радиотехнике, по содержанию примесей разделяется на
марки МО и М1. МО содержит 99,95% меди,
М1 – 99,90%. Эти марки обладают свойствами:
· плотность – 8,9.103 кг/м3;
· температура плавления – 1083 °С;
· удельное сопротивление r - 1,7241.10-8 Ом×м;
· механическая прочность – высокая;
· обрабатываемость – хорошая.
В зависимости от вида
примеси увеличение содержания примесей в меди увеличивает удельное
сопротивление r:
|
Zn, Cd, Ag (0,5 % примесей) |
5% |
|
Ni, Sn, Al (0,5 %) |
25 – 40 % |
|
Be, As, Fe, Si, P (0,5 %) |
больше 55% |
Из меди изготовляют
токопроводящие жилы проводов и кабелей, токопроводящие детали радиоаппаратуры,
фольгированный гетинакс для печатных схем, проволоку, листы, ленты, полосы,
тонкую фольгу.
Медные сплавы
Бронзы – сплавы меди
с некоторыми металлами. Различают следующие бронзы: оловянные,
алюминиевые, свинцовые, кремниевые, марганцевые, бериллиевые, кадмиевые и др.
Применение бронз:
·
кадмиевые –
для контактов и коллекторных пластин;
·
фосфористая –
для пружин в приборах и аппаратах;
·
бериллиевая –
для токоведущих пружин, щеткодержателей, скользящих контактов, электродов,
зажимов;
·
оловянистая – ее
называют телефонной т.к. из нее изготовляют проволоку для телефонных кабелей.
Латуни –
медно–цинковые сплавы. Из них изготовляют листы и полосы. Свойства латуни.
Удельное сопротивление латуни больше удельного сопротивления меди rлат > rмеди. Она способна удлиняться, сохраняя более высокую прочность,
чем медь. Поэтому она находит широкое применение в качестве конструкционного и
проводникового материала. Из нее изготовляют проводниковые детали резисторов,
конденсаторов, катушек, монтажные элементы схем.
Алюминий
Стоит на II месте после Cu
по применению в электро- и радиотехнике.
Плотность
Al в 3,5 меньше
плотности Cu
и равна примерно (2,6 ¸ 2,7) 103
кг/м3,
удельное сопротивление r в 1,68 раза больше, чем у Cu, r = 2,85 10-8 Ом×м. Примеси (Ti, Mn,
Cu,
Ag,
Mg) в алюминии снижают электропроводность (примерно
на 10%).
Для электротехники и
радиотехники применяют алюминий с содержанием примесей не более 0,5%;
для изготовления алюминиевой фольги для электролитических конденсаторов не
более 0,05%.
Тепловые свойства алюминия
|
Температура, °С: |
|
|
плавления– |
660 - 657; |
|
кипения
- |
2300 - 2500; |
|
отжига
- |
350 - 400; |
|
литья - |
700 - 750. |
Алюминий легко
окисляется на воздухе:
4Al +
3O2 ® 2Al2O3
и при действии серной
и щавелевой кислот (H2SO4, H2C2O4)
![]() .
.
Оксидная пленка на
поверхности алюминия защищает его от дальнейшего окисления (пассивация).
Промышленное оксидирование алюминия создает антикоррозийное и
электроизоляционное покрытие, которое часто сочетают с окраской и полировкой
для улучшения внешнего вида. Пробивное напряжение таких покрытий доходит до 400
В, (Uпр
= 400 В).
Но пленка Al2O3 затрудняет пайку и создает большое сопротивление в
контактах. При действии влаги в местах контакта Al-Cu
образуется гальванопара с высоким
значением э.д.с.
анод
Al½H2O; O2½Cu катод
ja = -1,7 B Aнод(+): Al0 - 3eˉ ® Al3+ Kатод(-): 2H2O
+ O2 + 4eˉ ® 4OHˉ jk
= - 0,83
B
Al3+ + 3OH ® Al(OH)3
При этом алюминиевый
проводник разрушается.
Для проводов
воздушных линий с большим натяжением и нагрузкой применяется алюминиевый сплав альдрей, который состоит:
(98,5
¸
99%)Al + (0,3 ¸ 0,5%)Mg + (0,4 ¸ 0,7%)Si + (0,2 ¸ 0,3%)Fe
Повышение
механической прочности достигается термообработкой, возрастает прочность на
растяжение до
Для передачи энергии
применяются сталеалюминиевые провода, в котором центральные жилы стальные, а
наружные – алюминиевые.
Железо и стали
Стали, используемые в
основном в качестве конструкционного материала и магнитного материала в
сердечниках трансформаторов, обладают более высоким удельным сопротивлением r по сравнению с
медью, около 10.10‾8 Ом×м. В качестве проводникового материала применяют сталь, с
содержанием углерода 0,1 ¸ 0,15 % с r в 6–7 раз
больше, чем у меди. Ее используют для проводов воздушных линий передач
небольших мощностей на короткие расстояния. Для предохранения от коррозии
провода и изделия из стали покрывают цинком.
Свинец
Мягкий, пластичный,
мало прочный металл, с низкой вибростойкостью. Температура плавления 327 °С.
Удельное сопротивление r = 2, 4, 1 мкОм×м при температурах t = 0, 200,
350 °С, соответственно.
Свинец ядовит.
Антикоррозийность высокая. Применяют в качестве защитных оболочек в кабельной
промышленности, плавких предохранителей, пластин свинцовых аккумуляторов,
поглотителей рентгеновских лучей и радиоактивных излучений. По мере возможности
вытесняется полихлорвинилом.
Олово
Чистое олово обладает крупнокристаллической структурой. При изгибе
слышен треск от трения кристаллов, что определяет чистоту металла. Температура
плавления 232 °С.
Благодаря мягкости и вязкости
из него изготовляют фольгу. Высокая антикоррозийность позволяет использовать
для защитных покрытий лужением или гальванизацией. Входит в состав бронз.
Применяют при пайке.
3.2.
Высоконагревостойкие металлы
С развитием вакуумной
техники, реактивной техники и применением радиоэлектронной аппаратуры в космосе
повысились требования к рабочим температурам, достигающим 2500 °С. В этих условиях в
качестве проводниковых и конструкционных материалов применяют тугоплавкие
металлы и их сплавы: вольфрам (W),
молибден (Mo),
тантал (Ta),
ниобий (Nb),
титан (Ti),
цирконий (Zr),
рений (Re).
Вольфрам
Вольфрам – тяжелый, твердый, наиболее
тугоплавкий металл. Добывается в основном из руд двух соединений: вольфрамит FeMnWO4
и шеелит CaWO4.
Руды сплавляют с
содой на воздухе, получают Na2WO4, который извлекают из сплава водой, а железо и марганец
превращаются в нерастворимые соединения Fe2O3
и Mn3O4.
Из водного раствора
действием HCl выделяют
свободную вольфрамовую кислоту H2WO4 в виде аморфного
желтого осадка:
Na2WO4 + 2HCl ® 2NaCl +
H2WO4¯
При прокаливании
вольфрамовая кислота переходит в WO3. Восстанавливая
оксид вольфрама водородом или углеродом (чистые сорта сажи), получают порошок металлического W. Порошок прессуют и спекают в бруски (штабики). Спекание в
атмосфере водорода проводят в две стадии.
Первая стадия –
предварительное спекание в водородных печах при 1100 – 1200 °С с целью повышения
механической прочности и электрической проводимости штабиков.
Вторая стадия –
высокотемпературное спекание при пропускании через штабик электрического тока,
постепенно нагревающего его до 3000 - 3200 °С.
При этом получается
компактный металл, поступающий на механическую обработку: ковку, протяжку.
W
– белый тяжелый металл плотностью 19,3.103 кг/м3, tпл
≈ 3400 °С.
Вольфрам можно сваривать и вытягивать в тонкие нити, прокатывать в листы.
Содержание вольфрама в металле не менее 99,5 %.
Максимальная рабочая температура в вакууме – 2560 °С, удельное сопротивление r = 0,055×мкОм×м, температура
испарения tисп = 5930 °С. Для
повышения чистоты вольфрама применяют метод электроннолучевой плавки и зонной
очистки. Из вольфрама изготовляется проволока, фольга, катоды накала мощных
генераторных ламп и кенотронов, сетки усилительных и генераторных ламп, вводы в
вакуумные приборы, контакты на большие мощности тока, нити ламп накаливания.
Сплавы вольфрама с
медью и серебром сочетают в себе высокие электропроводность, теплопроводность и
износоустойчивость. Они применяются для изготовления рабочих частей
рубильников, выключателей. Сплавы с кобальтом и хромом – стеллиты обладают высокой твердостью, износоустойчивостью,
жаростойкостью.
На воздухе вольфрам
окисляется при температуре красного каления. Стоек по отношению к кислотам,
даже к царской водке, но растворяется в горячей «адской»
смеси -смеси азотной и плавиковой (фтороводородной) кислот
W + 2HNO3 +
8HF
= H2[WF8]
+ 2NO
+ 4H2O
с образованием
октафторовольфрамовой (VI) кислоты.
Молибден
Молибден –
серебристо-белый металл. Добывают из руды молибденит или молибденовый блеск MoS2
(похож на графит).
Перерабатывая руду, получают MoO3. Восстановление MoO3 ведется в две стадии:
MoO3 + H2 → MoO2 + H2O
MoO2 + H2 → Mo
+ 2H2O
Получается
порошкообразный мелкозернистый (1 - 2 мкм) чистый металл с небольшим содержанием
кислорода и азота. Процесс получения молибдена аналогичен получению вольфрама.
|
Свойства молибдена: |
|
|
Плотность,
103 кг/ м3 |
9,7÷10,5 |
|
Температура
плавления, °C |
2622 ± 10 |
|
Максимальная
рабочая температура в вакууме, °C |
1700 |
|
Удельное
электрическое сопротивление, мкОм×м |
0,056 мкОм×м. |
Молибден химически
менее стоек, чем вольфрам. Начинает окисляться на воздухе при 400 °С.
Из молибдена
изготовляют катоды газоразрядных приборов, магнетроны, вводы для вакуумных приборов,
сетки для ламп, аноды. Выпускают в виде проволоки, листов, фольги, лент.
Растворяется в
азотной кислоте или горячей концентрированной серной кислоте.
Тантал и ниобий
Тантал и ниобий
близки по физическим и химическим свойствам. Добывают из руд танталит (Mn, Fe)(Ta, Nb)2O6
и колумбит
(Fe,
Mn)(Nb, Ta)2O6. Из них получают фтористые соли: фторотанталат калия и оксифторниобат
калия, являющиеся вторичными исходными материалами.
Восстановление Ta происходит в
реакции:
Тантал получают в
виде порошка. Аналогично получают ниобий.
Реакция
экзотермическая, проводится при 1000 °С во взрывобезопасном оборудовании.
Дальнейшая технология
изготовления заготовок и изделий из Ta и Nb
такая же, как из вольфрама и
молибдена. Выпускают оба металла в виде прутков, проволоки, листов, лент,
фольги. Методом зонной плавки производят также выращивание кристаллов.
В промышленности
методом порошковой металлургии изготовляют 5 марок Та:
Т – тантал повышенной
чистоты;
ТЧ – тантал высокой
чистоты;
ТН3 – сплав Та
и Nb;
ТН20 – сплав Та
и Nb;
ТТ1 – тантал
торированный.
Ниобий выпускается
одной марки.
|
Физические свойства |
Та |
Nb |
|
Плотность,
103 кг/м3 |
16,6 – 17 |
8,58 |
|
Температура
плавления, °С |
2990 ± 50 |
2415 |
|
Максимальная
рабочая температура, °С |
2200 |
2100 |
|
Удельное
сопротивление, мкОм× м |
0,15 |
0,13 |
Механические свойства
Та и Nb характеризуются высокой пластичностью.
Применение тантала в
электронной технике обусловлено его адсорбционной способностью, т.е. способностью
поглощать газы при 700 - 1800°С. Тантал применяют для изготовления катодов косвенного
накала с оксидноториевым покрытием в магнетронах. Тантал применяют для
изготовления анодов и сеток генераторных ламп, при изготовлении танталовых
конденсаторов.
Ниобий тоже обладает
адсорбционными свойствами при 400 ¸ 900°С, и его используют как газопоглотитель.
Оба металла, особенно
тантал, устойчивы в агрессивных средах. На них не действует HCl, H2SO4, HNO3, HСlO4 и царская водка, т.к. на поверхности этих металлов
образуется тонкая, но очень прочная и химически стойкая оксидная пленка (Та2О5, Nb2О5). Можно растворить в
горячей щелочи:
4Ta +
5O2 +
12KOH = 4K3TaO4
+ 6H2O
с образованием
танталата калия K3TaO4.
Или в ²адской²
смеси
3Ta +
21HF + 5HNO3
= 3H2[TaF7] + 5NO +
10H2O
с образованием
гептафторотанталовой (V) кислоты H2[TaF7].
Тантал и ниобий –
компоненты жаропрочных и коррозионностойких сплавов, применяемых в
промышленности и космической технике. Тантал не взаимодействует с живыми
тканями организма человека и не вредит им, поэтому он применяется в хирургии
для скрепления костей при переломах, а танталовыми нитями сшивают нервные
волокна. Ниобий дешевле тантала, поэтому сплавы ниобия и тантала конкурируют с
применением тантала.
Титан и цирконий
Титан очень
распространен, его содержание в земной коре (0,6 % масс) выше, чем меди,
свинца, цинка. Минералы, содержащие титан, находятся в природе повсеместно, это
ильменит – FeTiO3, рутил - TiO2, перовскивит - CaTiO3, титанмагнетит -FeTiO3·nFe3O4. Добывают термическим методом. Руду переводят в TiO2, а затем
подвергают хлорированию в присутствии углерода, связывающего кислород в СО:
TiO2
+ 2Cl2
+ 2C = TiCl4
+ 2CO
Получающийся хлорид Тi (lV) восстанавливают магнием:
TiCl4
+ 2Mg = Ti +
2MgCl2
,
а
образующуюся смесь подвергают нагреванию в вакууме. При этом магний и его
хлорид испаряются и осаждаются в конденсаторе. Остаток – губчатый титан
переплавляют, получая компактный ковкий металл.
Примеси кислорода,
азота, углерода резко ухудшают механические свойства титана, и даже превращают
его в хрупкий материал. Очистку и переплавку проводят в вакууме (иодидный
способ).
Цирконий добывают из циркона ZrSiO4 – силикат циркония и бадделинита
ZrO2. Для получения порошкообразного циркония используют реакцию:
ZrO2 +
2Ca =
Zr + 2CaO
Порошок циркония
прессуют в штабики.
Чистые сорта титана и циркония получают термической диссоциацией из иодистых соединений
TiJ4, ZrJ4.
Сплавы содержат от
0,55% до 0,915% Mo, Cr,
Al, Mg, W, Cu.
|
Свойства |
Иодидный
Тi |
Иодидный
Zr |
|
Плотность при 20 °С, 103 кг/м3 |
4,5 |
6,5 |
|
Температура плавления, °С |
1725 |
1845 |
|
Удельное сопротивление, мкОм×м |
0,48 |
0,41 |
Титан и цирконий
имеют малый коэффициент температурного расширения близкий к коэффициенту
температурного расширения керамики и стекла. Иодидные металлы высокой чистоты
отличаются малым электросопротивлением и меньшими механическими свойствами по
сравнению с техническими сортами металлов.
На поверхности титана
имеется плотная защитная пленка, стойкая против коррозии. Поэтому коррозионная
стойкость титана превышает стойкость нержавеющей стали. Титан не окисляется на
воздухе, в морской воде, в разбавленной и концентрированной азотной кислоте и
царской водке, но в НСl растворяется:
6HCl +
2Ti = 2TiCl2
+ 3H2
Главное свойство
титана и его сплава с алюминием – высокая жаростойкость наряду с высокими механическими
свойствами при высоких температурах. Его используют в самолето- и
ракетостроении. Титан немного тяжелее алюминия, но в 3 раза прочнее.
Примеси кислорода, азота и водорода резко повышают твердость,
прочность, снижают удлинение и пластические свойства титана. Из титана и его
сплавов изготовляют листы, прутки, фольгу. Титан и цирконий способны хорошо
поглощать газы (водород, кислород, азот) и удерживать их в широком диапазоне
температур. В вакуумной технике из титана и циркония изготовляют аноды, сетки и
др. детали, работающие при высокой температуре.
Рений
Рений – относится к
группе редких металлов и не образует самостоятельных минералов. Его получают
при переработке молибденовых и медных руд, в которых он содержится в малых
количествах. Технический рений получают из перрената
калия восстановлением водородом при
600 – 1000 °С:
KReO4
+ 3,5H2
= Re + KOH
+ 3H2O
Затем его в виде
порошка прессуют в штабики и подвергают
предварительному обжигу при 1200 °С под вакуумом, чтобы избежать окисления Re
до Re2О7. Окончательный обжиг и полное спекание производят при t
= 2800 °С в водороде.
|
Свойства рения: |
|
|
Цвет металла
|
светло – серый |
|
Плотность,
103 кг/м3 |
21 |
|
Температура
плавления, °С |
3176,6 |
|
Температура
испарения, °С |
5900 |
|
Удельное
сопротивление, мкОм×м |
0,21 |
Рений обладает
высокой кислотостойкостью. Применяется для изготовления катодов в газоразрядных
приборах, генераторных лампах, изготовления сеток, подогревателей и др.
Сплавы тугоплавких
металлов, применяемые в электронной технике и технике связи: W
– Mo,
Mo - Re, W
- Re,
Ta - Nb, Ta
– W.
Они характеризуются высокой температурой плавления (до 3000 °С), высокой
рабочей температурой (до 2500 °С), высокой механической прочностью,
пластичностью, твердостью. Применяют в вакуумной технике.
Благородные металлы:
серебро (Ag), золото (Au), платину (Pt), палладий (Pd) - получают из руд, но встречаются также и в самородном
состоянии.
Серебро
Самая важная серебряная руда – серебряный блеск или аргентит
Ag2S. В
качестве примесей серебро присутствует в медных и свинцовых рудах. Из этих руд
получают 80% всего
добываемого серебра.
Серебро очень мягкий, тягучий металл, лучше всех металлов
проводит теплоту и электрический ток. Вследствие мягкости на практике в чистом
виде не применяют, обычно сплавляют с медью и изготовляют ювелирные и бытовые
изделия, монеты. Чистое серебро используется для покрытия других металлов, а
также радиодеталей в целях повышения их электрической проводимости и
устойчивости к коррозии.
Золото
Золото – встречается
в самородном состоянии в виде мелких зерен, вкрапленных в кварц, или
содержащихся в кварцевом песке. В небольших количествах золото встречается в
сульфидных рудах железа, свинца и меди.
Золото отделяется от
песка и измельченной кварцевой породы промыванием водой, которая уносит частицы
песка, как более легкие, или обработкой
песка жидкостями, растворяющими золото:
4Au + 8NaCN + O2 + 2H2O = 4Na[Au(CN)2]
+ 4NaOH
Из полученного
раствора золото выделяют цинком:
2Na[Au(CN)2]
+ Zn = Na2[Zn(CN)4]
+ 2Au
Золото обрабатывают разбавленной серной кислотой для
отделения цинка, промывают и сушат. Дальше очищают от примесей золото электролизом
или горячей концентрированной серной кислотой. Этот способ, называемый
гидрометаллургическим, разработан в
Золото – ярко-желтый блестящий металл,
очень ковок и пластичен, из 1 г золота можно вытянуть проволоку длиной 3,5 км.
Очень хорошо проводит теплоту и электрический ток, но уступает по
электропроводности и теплопроводности серебру и меди.
Серебро и золото в чистом виде или в виде сплавов применяют
в качестве припоев в приборах. Используются для защиты изделий от коррозии.
Палладий
Палладий – обладает ценным для
электровакуумной техники свойством – поглощать водород. Коэффициент поглощения
доходит до 850, т.е. 1 объем палладия поглощает 850 объемных единиц водорода.
Платина
Платина – химически стойкий, не соединяющийся
с кислородом металл. Хорошо поддается обработке, вытягивается в нити и ленты.
Применяется для термопар в паре с платинородием (Pt – Rh) для измерения температур до t = 1600 °С.
Платиноиридиевые сплавы (Pt – Ir)
не окисляются, имеют высокую твердость и износ.
|
Свойства благородных металлов |
||||
|
|
Au |
Ag |
Pt |
Pd |
|
Плотность,
103 кг/м3 |
19,3 |
10,55 |
21,45 |
12,02 |
|
Температура
плавления, °С |
1063 |
960,8 |
1773 |
1554,4 |
|
Удельное
сопротивление, мкОм·м |
0,0235 |
0,0147 |
0,106 |
0,108 |
3.4. Металлы и
сплавы различного назначения.
Никель
Никель встречается в
природе в виде соединений с мышьяком или серой – купферникель NiAs; мышьяковоникелевый блеск – NiAsS. Из этих соединений никель извлекают в сульфиды, называемые штейн. Наиболее чистый никель получают
электролитическим и карбонильным способом.
Электролитический
способ заключается в осаждении никеля на катоде (при электролизе соли никеля с
никелевым анодом), а карбонильный – в разложении карбонила никеля Ni(СО)4
при высокой температуре и выделении чистого никеля в виде порошка.
Как проводник никель
обладает такими ценными свойствами:
♦ малая
окисляемость на воздухе;
♦
антикоррозийность;
♦
хорошая обрабатываемость.
Никель выпускается 5
марок:
Н0 (99,99% Ni), Н1 (99,93% Ni),
Н2 (99,8% Ni), Н3 (98,6% Ni), Н4 (97,6% Ni).
Допускаются примеси C, Mg, Si, P, S, Mn, Fe, Bi, Cu, Zn, Cd, Sn, Pb, Co – содержанием не более 0,01%.
Никель выпускается в
виде проволоки, листов, фольги, лент, полос,трубок.
|
Свойства никеля |
|
|
Плотность,
103 кг/м3 |
8,9 |
|
Температура
плавления, °С |
1452 |
|
Удельное
сопротивление, мкОм·м |
0,068 |
Никель химически
стойкий, малоактивный металл. Широко применяется в производстве
электровакуумных приборов в виде бесшовных трубок, полос, проволоки; для изготовления
сеток маломощных приемоусилительных ламп, анодов генераторных ламп; для
гальванического антикоррозийного покрытия железа, меди, латуни.
На основе никеля
создано большое число ценных сплавов:
|
жаропрочные |
нимоник (59% никеля, остальное хром, кобальт
и др.) инконель (73% никеля, остальное кобальт,
железо и др.) нихром (60% никеля, остальное хром, железо
и др.) алюмель (сплав никеля с алюминием,
марганцем, кобальтом, кремнием) |
|
химически
стойкие |
монель (65% никеля, остальное медь и др.) |
|
магнитные |
пермаллой (78,5% никеля + 21,5% железа) – для
изготовления сердечников трансформаторов инвар (36% никеля + железо и др.) –
практически не расширяется при повышении температуры до 100°С. |
Ртуть
Ртуть – получают из сернистой
ртути (киновари) нагреванием на
воздухе при ≈ 500 °С:
Hg + O2 = Hg + SO2
Получающийся металл –
жидкий, серебристо-белого цвета, содержит примеси Pb,
Bi, Zn, Sn и др.
|
Свойства
ртути |
|
|
Плотность,
103 кг/м3 |
13,5 |
|
Температура
плавления, °С |
– 38,89 |
|
Давление
насыщенных паров, мм рт.ст |
1,3·10-3 |
|
Удельное
сопротивление, мкОм·м |
0,958 |
Наиболее важное
свойство, используемое в вакуумной технике, это высокое давление насыщенных паров
ртути и скорость их испарения, что делает возможным работу вакуумных приборов с
ртутным заполнением.
Ртуть – химически
стойкий металл, окисляется на воздухе при 300°С. Некоторые металлы (Al, Mg, Sn, Pb, Cd, Zn, Ag, Au, Pt) растворяются в ртути, образуя амальгамы. Fe, W, Ta – не растворяются в ртути. Не взаимодействует с ртутью
графит, стекло, керамика, слюда.
Ртуть применяют в
газоразрядных приборах, где используется ионизация паров ртути; в ртутных
выпрямителях; для контактов в приборах автоматического включения (реле и др.).
К щелочным металлам относятся литий (Li), натрий (Na),
калий (K), цезий (Cs), рубидий
(Rb) – элементы I группы периодической системы. Натрий и калий получают
электролизом расплавов:
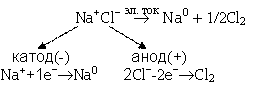
Cs, Li, Rb – получают восстановлением металлическим цирконием из
хромовых солей:
Cs2CrO4
+ Zr ®
Cs + ZrCrO4
Rb2CrO4
+ Zr ®
Rb + ZrCrO4
Li2CrO4 + Zr ® Li + ZrCrO4
|
|
Na |
K |
Cs |
Li |
Rb |
|
Плотность, 103
кг/м3 |
0,97 |
0,86 |
1,87 |
0,5 |
1,53 |
|
Температура
плавления, °С |
98 |
63 |
28 |
186 |
39 |
|
Температура
кипения, °С |
883 |
776 |
690 |
1370 |
700 |
|
Удельное
сопротивление, мкОм×м |
0,042 |
0,062 |
0,19 |
0,086 |
0,125 |
|
Работа выхода
электронов, эВ |
2,27 |
2,1 |
1,89 |
2,3 |
2,1 |
Применение щелочных
металлов в электровакуумной технике основано на высокой светочувствительности
при малом значении работы выхода электронов (Cs обладает даже чувствительностью к ИК - лучам). Применяют
для фотоэлектронных катодов, фотоэлементов, фотоумножителей, для рентгеновских
трубок.
Щелочные металлы
химически активны. С кислородом реакция идет бурно, со взрывами. Легко
воспламеняются. Нельзя тушить углекислотой:
Na2O + CO2 = Na2CO3
Необходимо соблюдать
меры безопасности: хранить эти металлы под слоем керосина, применять защитные
очки, работу производить в сухом помещении.
Щелочноземельные
металлы барий (Ва),
стронций (Sr), кальций
(Ca)
– элементы второй группы периодической системы.
Добывают из барита – BaSO4, витерита – ВаСО3, целестина – SrSO4, стронцианита – SrCO3, известняка, мрамора, мела – СаСО3, гипса – СаSО4.
Свойства щелочноземельных
металлов
|
|
Ba |
Sr |
Ca |
Mg |
|
Плотность, 103
кг/м3 |
3,74 |
2,63 |
1,55 |
1,73 |
|
Температура
плавления, °С |
704 |
771 |
849 |
651 |
|
Температура
кипения, °С |
1537 |
1366 |
1487 |
1107 |
|
Удельное
сопротивление, мкОм×м |
0,50 |
0,23 |
0,034 |
0,0446 |
|
Работа
выхода, эВ |
2,29 |
2,35 |
2,76 |
3,46 |
При невысоких
температурах щелочноземельные металлы и магний имеют высокое давление
насыщенных паров и высокие скорости испарения. Они распыляются в вакууме и
осаждаются на поверхностях приборов.
Применяют
щелочноземельные металлы для оксидных катодов, поглотителей газов в вакуумных
приборах, стабилизаторов сеточных и анодных токов в радиолампах.
3.7. Сплавы
сопротивления и сплавы для термопар
Сплавы сопротивления применяются в электроизмерительных
приборах, реостатах, резисторах, электронагревательных приборах. Наибольшее
применение нашли:
Манганин (от марганца - манганум) – сплав меди,
марганца, никеля (86 % Сu+12 % Mn+2 % Ni). Удельное
сопротивление, r
– 0,42 ¸ 0,48 ; плотность– 8,4×103 кг/м3. Изготавливают в виде проволоки.
Константан – медно-никелевый
сплав. Удельное сопротивление r = 0,45¸0,52 мкОм×м. Выпускается в виде проволоки и лент. Проволока двух
сортов:
мягкая (М) и твердая (Т) - предназначена для работы при температурах до 500 °С и применяется для
реостатов. В паре с медью дает большую термо-э.д.с., что препятствует широкому
применению константановых резисторов в измерительных схемах. Используется для
изготовления медь – константановых термопар, для измерения температур порядка
600°С.
Нихромы или
хромоникелевые сплавы Х15Н60, Х20Н80
– жаростойкие сплавы. Из них изготовляют нагревательные элементы электропечей,
паяльников, электронагревателей. Из этих сплавов делают холоднотянутую и
горячекатаную проволоку и ленту.
Удельное
сопротивление нихрома r = 1¸1,2 мкОм×м, рабочая
температура t
= 1100 °С/
Увеличение содержания
хрома ухудшает обработку, повышает твердость сплава, но зато увеличивает
удельное сопротивление, повышает стойкость к окислению.
С целью удешевления и
улучшения механических свойств (прокатка, ковка) в нихром вводят железо. Но оно понижает рабочую температуру
сплава.
Нихром имеет оксидную
пленку на поверхности, поэтому у него продолжительный срок службы при
непрерывном нагреве. Если чередуется нагрев с охлаждением, то защитная пленка
растрескивается и происходит газовая коррозия, при которой уменьшается сечение
проводника, увеличивается местный нагрев, а провод перегорает от перегрева.
Фехраль и хромаль – сплавы
железа, хрома и алюминия. Дешевые, т.к. не содержат дефицитный никель, но более
твердые и хрупкие, менее технологичные при изготовлении проволоки и лент.
Проволоку делают крупных сечений и применяют для мощных электропечей, муфельных
печей.
Удельное
сопротивление,– 1,3 мкОм×м.
Сплавы для термопар
Для изготовления
термопар применяются сплавы.
·
Копель – 56 % Сu + 44 % Ni.
В паре с медью применяется до 350 °С; с
железом, хромелем до 600 °С.
·
Константан -
60 % Сu
+ 40 % Ni. В паре с медью применяется до 350°С; с железом до 600 °С;
·
Хромель –
90 % Ni
+ 10 % Сr.
Дешевый сплав, в паре с алюмелем применяется до 900 – 1000 °С
·
Алюмель – 95 % Ni + 5 % Аl.
Дешевый сплав для температур до 900 – 1000 °С.
·
Платинородий
– 90 % Рt + 10 % Rh. Дорогой сплав, в паре с платиной применяется при
температурах до 1600 °С.
Наибольшей
термо-э.д.с из перечисленных термопар на один градус обладает хромель копель –
около 80 мкВ/град
3.8. Металлы и
сплавы электровакуумной техники
На основе металлов со средней температурой плавления (Fе, Ni) созданы сплавы, которые широко применяются
в электровакуумных технологиях. Эти сплавы обладают согласованным со стеклом
коэффициентом линейного температурного расширения и позволяют получать
совмещенные со стеклом металлические изделия и спаи со стеклом.
Инвар
Сплав 36 % никеля и 64 % железа, практически не расширяется при
нагревании до 100°С и применяется в электрорадиотехнике и в химическом
машиностроении.
Платинит
Сплав 47 % никеля и железа (Н47). Имеет коэффициент температурного
расширения такой же, как у стекла и используется для впаивания вводов
металлических контактов в стекло (коэффициент линейного температурного
расширения платинита примерно равен стеклу).
Ковар
Сплав железа с 29%
никеля и 17% кобальта. Удельное сопротивление ковара в два раза меньше
сопротивления инвара.
Инвар и ковар применяют
для герметизации изделий путем сварки со стеклом, для изготовления
конденсаторов с переменной емкостью.
Электрические контакты, применяемые в различных установках, аппаратах
разделяют на три группы.
·
Разрывные
контакты предназначены для размыкания и замыкания электрической цепи. Нарушение
работоспособности контактов обусловлено в зависимости от силы тока эрозией,
коррозией (окислению) и свариванием. Перенос металла, вызывает на одном контакте
нарост, а на другом – образование кратеров. Окисление повышает сопротивление
контакта вплоть до полного нарушения
проводимости. Спекание наблюдается при импульсах тока на маломощных контактах.
Для разрывных
контактов маломощных контактов прецизионных реле и приборов применяют: Pt, Pd, Au, Ag, W, Mo, Ni, Cu, Cu-Cd, Pt-Rh, Pt-Ir, Pt-Ru, Pt-Ni, Pt-W, Pd-Ir, Pd-Ag, Pd-Cu, Au-Ag, Au-Ni, Au-Zr, Ag-Cu, Ag-Cd. Особо ценными являются сплавы палладия с серебром и медью.
·
Скользящие
контакты применяются в ползунках потенциометров, обмотках резисторов, контактных
кольцах. Контакты должны быть стойки к истиранию, иметь низкое
электросопротивление. В контактах используют нихром, константан, Rh, Pd - Cu, Pd - Ir, Pd – Ag – Au – Cu, Pt - Ag, Ag, Ag - Pd, Cu - Cd.
·
Неподвижные
контакты используются в сигнальной аппаратуре (Ag, Pd-Ag, Pd-Cu, Ag-Cu); реле (Pd-Cu, Ag, Ag-Cu),
термостатах (Ag, Ag-Pd, Ag-Cd, Pt-Ir),
бытовых приборах (Аg),
низковольтных выключателях.
3.9. Металлокерамические контакты (керметы)
В аппаратах, где
происходит оплавление, приваривание или быстрый износ контактов, изготовленных
из чистых металлов и сплавов, рекомендуется применять контакты из
металлокерамических композиций (керметы), представляющих механическую смесь
несплавляющихся между собой компонентов.
Керметы получают
спеканием смесей порошков металлов и неметаллических компонентов – тугоплавких
оксидов, карбидов, боридов и др. Их прессуют из смеси порошков заданного
состава с последующим спеканием. Это: Ag - W; Ag – карбид вольфрама; Ag - Mo; Ag - Ni; серебро – оксид кадмия; серебро - графит; Cu – W. Часто в качестве металлической составляющей используют
металлы подгрупп Сr
и Fе.
Эти материалы
сочетают в себе тугоплавкость, твердость и жаростойкость керамики с
проводимостью, пластичностью и другими свойствами металлов.
Припои
Припои – сплавы для пайки металлов высокой проводимости. Для получения
хорошего соединения припой должен иметь температуру плавления ниже, чем у
металла, хорошо смачивать поверхность в расплавленном состоянии, иметь
небольшое сопротивление контакта. Температурные коэффициенты линейного
расширения металла и припоя должны быть близки друг к другу. Применяют припои
оловянно – свинцовые (ПОС - 61, содержащий 61 % олова, остальное - свинец), оловянно – цинковые (ПОЦ – 90, имеет температуру плавления
199 °С и используется
для пайки алюминия и его сплавов), сплавы висмута со свинцом, оловом, кадмием (для температур нагрева меньше, чем 100°С) и др.
Подразделяются:
·
мягкие припои
– температура плавления до 400 °С;
·
твердые припои
– температура плавления выше 500 °С.
Мягкие изготовляют
оловянно – свинцовые (ПОС) 18 % - 90 %. Существуют мягкие припои с содержанием висмута и кадмия,
алюминия, серебра – температура пайки до 140°С. Висмутовые припои очень хрупки. Широко применяют ПОС – 40
и ПОС – 60 (60 % и 40 % - олова).
Среди твердых припоев
наиболее распространены – медно – цинковые – ПМЦ и серебряные (ПСр).
Флюсы
Для облегчения пайки и обеспечения
надежности используют вспомогательные вещества – флюсы, которые должны:
1) растворять и удалять
оксиды с поверхности металлов;
2) защищать поверхность
металла от окисления;
3) улучшать
растекаемость припоя и смачиваемость спаиваемых поверхностей.
Флюсы подразделяются
на несколько групп:
1.
Активные
или кислотные флюсы – НСl, хлористые и фтористые соединений металлов.
В электротехнике и в радиотехнике не применяют.
2.
Бескислотные
флюсы – канифоль и флюсы на ее основе с добавкой неактивных веществ (спирт,
глицерин).
3.
Активированные
флюсы – канифоль с добавками солянокислого или фосфорнокислого анилина,
салициловой кислоты и др.
4.
Антикоррозийные
флюсы получают на основе фосфорной кислоты Н3РО4 с добавлением органических соединений и растворителей,
которые не вызывают коррозии.
Контактолы
Контактолы
применяются для получения контактов между металлами, металлами и
полупроводниками, создания электродов, экранирования от помех.
Контактолы готовятся в виде пасты на основе мелкодисперсного
порошка серебра, никеля, палладия, которые используются в качестве проводящей
фазы, взвешенной в высокомолекулярных веществах.
Водная паста высокодисперсного графита известна под названием аквадаг.
Неметаллические
проводники на основе углерода называют электроугольными изделиями.
Из электроугольных
изделий изготавливают:
·
электрические
щетки для коллекторов электромашин;
·
электроугли и
электроды, применяемые в дуговых лампах и электропечах;
·
электроды в
гальванических элементах;
·
угольные
мембраны для микрофонов, микрофонные порошки;
·
высокоомные
резисторы.
Основное сырье для
производства электроугольных изделий: графит, нефтяной кокс, пековый кокс, антрацит, сажа,
каменноугольная смола.
Электрощетки
являются скользящими контактами на коллекторе электрической машины и служат для
подвода и отвода тока. Щетки должны иметь малое сопротивление, малый износ,
хороший контакт с поверхностью коллектора. Щетки подразделяют на 4 группы:
|
1. |
угольно –
графитовые(Т2, УГ2), мкОм×м |
21¸54 |
|
2. |
графитные (Г1,
Г3)
мкОм×м |
12¸37 |
|
1. |
электрографитированные
(ЭГ2а,
ЭГ4, ЭГ8, …),
мкОм×м |
10¸50 |
|
2. |
металлографитные
(М1,
М3, …):
медные, или бронзо–графитные, мкОм×м |
0,2¸9 |
Изготавливаются щетки
прессованием в пресс-формах из измельченной углеродной массы. Для уменьшения
сопротивления массу могут добавляться порошки меди или бронзы. Заготовки
подвергаются обжигу. Обжиг ведут при температуре около 800 – 1000 °С. Так как при
высоких температурах углерод превращается в графит, то для получения
графитированных щеток обжиг проводят при температуре около 2200 °С
Электроугли служат:
1.
нагревательными
элементами электрических печей, где они выполняют роль резисторов;
2.
проводниками
электроэнергии к нагревательному элементу;
3.
электродами
вольтовой дуги;
4.
осветительными
углями в виде стержней в прожекторной, кинопроекционной, киносъемочной
электроаппаратуре.
Микрофонные порошки
Свойство угольного порошка изменять свое сопротивление в зависимости от
давления обусловливается переходным сопротивлением зерен порошка и используется
в микрофонах, где под действием звуковых колебаний изменяется давление на
порошок. Порошок изменяет свое сопротивление, что создает колебания тока в
электрической цепи.
Сырьем для порошков служит
антрацит, который дробится на куски £ 5мм, просеивается через сито (80 меш), обжигается в печах при 900 - 1000°С или 1480°С (в
зависимости от марки) и еще раз просеивается через сито (45
меш),
удельное сопротивление 0,40 – 7,0 Ом×м.
Мембраны для
микрофонов производят из смеси пекового кокса (75%) и каменноугольной
смолы (25%). Пек размалывают в
шаровой мельнице, просеивают через сито (100 меш), перетирают 24 часа на бегунах, просушивают в сушильных
барабанах, просеивают через сито (50 меш). Затем смешивают со смолой, прогретой до температуры 300 -
315°С.
Смесь обрабатывают на вальцах, размалывают в шаровых мельницах, просеивают
через сито (200 меш). Из полученного порошка на гидравлических прессах под
давлением прессуют мембраны в виде дисков и обжигают при температуре 1480°С.
Резисторы
Резисторы на основе
углерода (ВС, УЛИ и др.) отличаются от проволочных резисторов меньшими
размерами, высоким верхним пределом номинального сопротивления. В качестве
проводящего материала углеродистых резисторов используются природный графит,
сажа, пиролитический углерод[1],
бороуглеродистые пленки, полученные пиролизом бороорганических соединений.