5.1. Химическое равновесие в гомогенных системах
При равенстве энтальпийного и энтропийного факторов ΔН = ТΔS ΔG = 0, что является термодинамическим условием химического равновесия. Химическое равновесие имеет динамический характер. Скорость реакции (число частиц образующихся в единицу времени в единице объема) в прямом направлении равна скорости реакции в обратном направлении. В этот момент концентрации исходных веществ и продуктов реакции не изменяются во времени и называются равновесными концентрациями. Они обозначаются символом вещества в квадратных скобках.
5.1.1. Константа химического равновесия
При равновесии химической реакции:
bB + dD = lL + mM
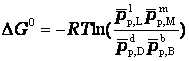
или
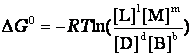 ,
,
где pp,L, ppM, pp,D, ppB –равновесные парциальные давления веществ, а [L], [M],[D],[B] –равновесные концентрации веществ; l, m, d, b - показатели степени, равные стехиометрическим коэффициентам.
Отношения произведений парциальных давлений или концентраций получили названия констант химического равновесия соответственно Кр или Кс:
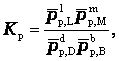
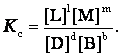
Эти уравнения являются математическими выражениями закона действующих масс, открытого норвежскими учеными К. Гульдбергом и П. Вааге в 1867 г.:
отношение
произведения равновесных концентраций продуктов реакции в степенях, равных
стехиометрическим коэффициентам, к произведению равновесных концентраций
исходных веществ в степенях, равных стехиометрическим коэффициентам, при Т
= соnst, является величиной постоянной.
Например, для реакции синтеза аммиака:
N2 + 3H2 = 2NH3
закон действующих масс имеет вид:
Кс = [NH3]2 / [N2][H2]3
Подставляя выражение константы в уравнения, получаем
ΔG0 = - RTlnKc = - 2,3RTlgKp,
ΔG0 = - RTlnKp = - 2,3RTlgKc.
Рассчитав величину ΔG0 химической реакции, можно определить константу химического равновесия. Используя закон действующих масс, можно рассчитать равновесные концентрации реагирующих веществ.
5.1.2. Влияние
температуры на константу равновесия
Из вышеприведенного уравнения следует
lnКс = - ΔG0/RT.
Энергия Гиббса процесса имеет значение ΔG0 = ΔH – TΔS. Тогда
lnKc = - ΔH0/(RT) + ΔS0/R.
Если ΔН и ΔS не зависят от температуры, то производная константы равновесия по температуре будет равна:
d(lnKc)/dT = ΔH0/(RT2).
Это изобара равновесия. Она показывает, что константа равновесия экзотермической реакции уменьшается, а эндотермической реакции возрастает с повышением температуры. С увеличением абсолютного значения энтальпии реакции и уменьшением температуры чувствительность константы равновесия (d(lnKc)/dT) к изменению температуры повышается.
5.1.3. Принцип Ле Шателье
При изменении равновесных концентраций исходных веществ и продуктов реакции путем воздействия на систему происходит смещение химического равновесия. Если увеличиваются равновесные концентрации продуктов реакции, то говорят о смещении равновесия вправо. Если при внешнем воздействии увеличиваются концентрации исходных веществ, то говорят о смещении равновесия влево.
Характер смещения равновесия можно прогнозировать, применяя принцип французского ученого Ле Шателье:
если на
систему, находящуюся в равновесии, оказывается внешнее воздействие, то
равновесие смещается в том направлении, которое ослабляет внешнее воздействие.
Принцип Ле Шателье следует из закона действующих масс. Если система находится при постоянной температуре, то константа равновесия при внешних воздействиях остается постоянной. Поэтому любое изменение равновесных концентраций веществ должно приводить к такому изменению равновесных концентраций других веществ, чтобы соблюдалось постоянство константы равновесия.
Рассмотрим процесс конверсии метана:
CH4 + 2H2O = CO2 + 4H2,
Константа равновесия этого процесса имеет вид:
Кс = [CO2] [H2]4/[CH4] [H2O]2.
1. Рассмотрим, как влияет изменение концентраций на смещение равновесия. При увеличении концентрации метана СН4 равновесие системы нарушается, идет прямая реакция. Концентрации продуктов реакции СО2 и Н2 увеличиваются, а концентрации Н2О уменьшается. Процесс будет протекать до тех пор, пока не установится новое равновесие. Новые равновесные концентрации компонентов будут такими, что константа равновесия не изменится. Если увеличить концентрацию СО2, то по принципу Ле Шателье равновесие сместится влево.
2. Если в результате реакции изменяется число молей газообразных веществ, то изменяется общее давление в системе и происходит смещение равновесия. В соответствии с принципом Ле Шателье увеличение общего давления вызывает смещение равновесия в сторону уменьшения числа молей газообразных веществ, т.е. в сторону уменьшения давления. Для рассматриваемой реакции увеличение давления должно смещать равновесие влево (слева- 3 моля, справа – 5 молей).
3. С увеличением температуры равновесие смещается в сторону эндотермических реакций, т.е. реакций протекающих с поглощением теплоты, понижение – в сторону экзотермических реакций.
Итак, принцип Ле Шателье позволяет создавать такие условия протекания реакции, которые обеспечивают максимальный выход продуктов реакции.
5.2. Химическое равновесие в гетерогенных системах
Химические реакции, протекающие на границе раздела фаз, называются гетерогенными химическими реакциями.
При равенстве скоростей прямой и обратной реакции наступает химическое равновесие в гетерогенной системе. Примерами гетерогенных процессов является пароводяная конверсия углерода, или восстановление оксидов металлов водородом:
С(к) + 2Н2О
= СО2 + 2Н2 ,
МеО(к) + Н2 = Ме(к) + Н2 О.
Как и для любого равновесия, условием гетерогенного химического равновесия является равенство энергии Гиббса нулю, ΔG = 0.
5.2.1. Константа равновесия гетерогенной реакции
Как и в случае гомогенной химической реакции, константа гетерогенного равновесия равна отношению произведения равновесных концентраций (активностей) или парциальных давлений продуктов реакций к произведению равновесных концентраций (активностей) или парциальных давлений исходных веществ в степенях, равных стехиометрическим коэффициентам в уравнении. Для реакции пароводяной конверсии углерода константа равновесия имеет вид:
Кр = (рСО2)р (рН2)2р/(рН2О)2р,
для восстановления металла
Кр = (рН2O)р/(рН2)р.
Из приведенных выражений следует, что в уравнения констант гетерогенного химического равновесия не входят концентрации твердых веществ, участвующих в прямой и обратной реакциях. Это особенность гетерогенного химического равновесия.
Так как прямая и обратная реакции протекают на одной и той же поверхности раздела фаз, то площадь поверхности раздела фаз также не входит в уравнение константы химического равновесия.
Константа гетерогенного химического равновесия зависит от температуры. Она возрастает с увеличением температуры для эндотермической прямой реакции и уменьшается с увеличением температуры в случае экзотермической прямой реакции. Расчеты проводятся по тем же формулам, что и для гомогенных реакций.
Смещение равновесия гетерогенных реакций подчиняется принципу Ле Шателье. При повышении температуры оно смещается в сторону эндотермической реакции. При повышении давления или концентрации исходных веществ равновесие смещается в сторону образования продуктов реакции, при повышении концентрации или давления продуктов реакции равновесие смещается в сторону обратной реакции. При повышении общего давления равновесие сдвигается в направлении уменьшения числа молекул газообразных веществ.
Твердые исходные вещества и продукты реакции не влияют на смещение гетерогенного химического равновесия.
Одно и то же вещество может при изменении температуры и давления переходить в различные агрегатные состояния. Эти переходы, осуществляемые без изменения химического состава, называются фазовыми переходами. Если рассматривается гетерогенная система, в которой нет химического воздействия, а имеются лишь фазовые переходы, то при постоянстве температуры и давления существует так называемое фазовое равновесие. Примерами фазового равновесия могут быть процессы плавления, кристаллизации, испарения, конденсации воды. Это равновесие характеризуется некоторым числом фаз, компонентов и числом степеней термодинамической свободы системы или числом степеней свободы.
Фаза – это однородная часть системы одинаковая по составу и свойствам, имеющая поверхность раздела, и которая может быть выделена из системы чисто механическим путем.
Так, система лед+вода имеет две фазы.
Компонентом называется химически однородная составная часть системы, которая может быть выделена из системы и может существовать вне ее.
Так, в растворе хлорида натрия компонентами являются вода и хлорид натрия, но ионы натрия и хлора не могут считаться компонентами.
Число степеней свободы определяется как число параметров системы (температура, давление), которые могут быть произвольно изменены в некоторых пределах без изменения числа и природы фаз в системе.
У системы, состоящей лишь из газа, можно менять два параметра, третий система устанавливает произвольно сама.
Число степеней свободы определяется правилом фаз Дж.Гиббса (1876 г.):
число
степеней свободы равновесной системы, на которую влияют только температура и
давление, равно числу независимых компонентов системы минус число фаз плюс два:
С =
К – Ф + 2,
где С – число степеней свободы; К – число компонентов; Ф – число фаз; 2 – число независимых параметров, например температура и давление.
Классификацию систем можно проводить: по числу фаз (однофазные, двухфазные и т.д.); по числу компонентов системы (однокомпонентные, двухкомпонентные и т.д.); по числу степеней свободы – инвариантные (С = 0), моновариантные (С = 1), дивариантные (С = 2) и т. д. Диаграммы, по которым можно определить условия устойчивости фаз и фазового равновесия, называются фазовыми диаграммами или диаграммами состояния. Для однокомпонентных систем правило фаз имеет вид
С = 3 – Ф
Примером однокомпонентной системы
служит диаграмма состояния воды в координатах давление – температура.  (рис.15) Области, находящиеся между кривыми, являются
однофазными областями (С = 2). Кривые соответствуют условиям равновесия между
двумя фазами (С = 1). Кривая ОС отражает равновесие процесса кипения. Кривая
кипения оканчивается точкой С, которая называется
критической. При температуре выше этой точки невозможно получить жидкую воду ни
при каком давлении. Вода, при температурах выше критической и давлении, выше
критического, переходит в особое состояние, называемое сверхкритическим (СК).
Свойства веществ в этом состоянии находятся между свойствами газа и жидкости.
Например, вещества в сверхкритическом состоянии имеют очень низкую вязкость,
высокую диффузионную активность и способность растворять многие вещества в
твердом, жидком или газообразном видах.
(рис.15) Области, находящиеся между кривыми, являются
однофазными областями (С = 2). Кривые соответствуют условиям равновесия между
двумя фазами (С = 1). Кривая ОС отражает равновесие процесса кипения. Кривая
кипения оканчивается точкой С, которая называется
критической. При температуре выше этой точки невозможно получить жидкую воду ни
при каком давлении. Вода, при температурах выше критической и давлении, выше
критического, переходит в особое состояние, называемое сверхкритическим (СК).
Свойства веществ в этом состоянии находятся между свойствами газа и жидкости.
Например, вещества в сверхкритическом состоянии имеют очень низкую вязкость,
высокую диффузионную активность и способность растворять многие вещества в
твердом, жидком или газообразном видах.
Кривая ОВ – это кривая плавления. При увеличении давления температура плавления немного уменьшается, что обусловлено разрывом водородных связей при повышении давления.
Кривая ОА отражает процесс сублимации, т.е. перехода из твердого состояния в газообразное, минуя жидкое. Кривая ОД описывает поведение воды в неустойчивом (метастабильном) состоянии. Явление образования метастабильного состояния получило название переохлаждения.
В точке О существует равновесие одновременно между тремя фазами. Она называется тройной точкой воды, и для нее давление равно 610 Па и температура 273,15 К.
Процесс поглощения одного вещества поверхностью или объемом другого называется сорбцией.
Вещество, частицы которого поглощаются (газ, жидкость или растворенный компонент), называют сорбатом, а поглотитель (чаще твердое тело) – сорбентом.
Сорбционные процессы играют большую роль в технике. Например, для поддержания высокого вакуума в действующем электровакуумном приборе применяют геттеры – специально изготовленные материалы, которые активно поглощают остаточные газы. В качестве геттеров используют компактные (Zr, Ta, Nb и др.) или распыленные (Ba, Ca, Sr ) металлы. Сорбционные процессы широко используют в металлургии при обогащении руд (флотация), в энергетике при водоподготовке (ионный обмен) и др.
При контакте сорбент поглощает сорбат поверхностью или объемом. Сорбция только поверхностью называется адсорбцией, а только объемом – абсорбцией. Процесс обратный адсорбции называется десорбцией.
Адсорбция связана с особым энергетическим состоянием частиц на поверхности адсорбента в отличие от энергетического состояния частиц в его объеме. Частицы во внутренних слоях вещества испытывают одинаковое притяжение со стороны окружающих частиц по всем направлениям.
Частицы же поверхностного слоя подвергаются неодинаковому притяжению со стороны внутренних слоев вещества и со стороны частиц граничащей с веществом посторонней фазы. Поэтому частицы поверхностного слоя адсорбента обладают свободной поверхностной энергией, которая может быть снижена за счет возникновения абсорбционных взаимодействий с молекулами, атомами и ионами адсорбата.
Для границы раздела фаз жидкость – газ (пар) обычно используют термин "удельная (на 1 м2) поверхностная энергия", называемая поверхностным натяжением, которая равно работе образования единицы площади поверхности раздела фаз (Дж/м2).
Поверхностная энергия – это энергия Гиббса ΔG образования поверхности. Она равна произведению удельной поверхностной энергии σ на площадь поверхности раздела фаз S:
ΔG = σS.
Удельная поверхностная энергия зависит от природы вещества. Чем выше энергия взаимодействия между частицами вещества, тем выше удельная поверхностная энергия. С увеличением температуры удельная поверхностная энергия уменьшается.
В зависимости от природы сил взаимодействия адсорбирующего вещества с адсорбентом различают физическую и химическую (хемосорбцию) адсорбцию. В первом случае при адсорбции возникают вандерваальсовы взаимодействия, во втором – химические связи.
Физическая адсорбция характеризуется невысоким тепловым эффектом и обратимостью.
Хемосорбция протекает необратимо. Тепловой эффект ее близок к тепловому эффекту химических реакций.
5.4.2.
Термодинамика адсорбции
Поскольку адсорбция протекает самопроизвольно, то энергия Гиббса имеет отрицательное значение
ΔGадс < 0.
Тепловой эффект адсорбции имеет также отрицательное значение
ΔНадс < 0.
Если адсорбция протекает из газовой, жидкой фазы на поверхность жидкой или твердой фазы, то в процессе адсорбции происходит упорядочение адсорбированных частиц и энтропия системы уменьшается, т.е.
ΔSадс < 0.
Отсюда следует, что с увеличением температуры энергия Гиббса системы возрастает, и при некоторой температуре Тр наступает равновесие, в это время скорость адсорбции равна скорости десорбции. При этом
ΔGадс = 0 и TрΔSадс = ΔHадс.
При увеличении температуры адсорбция уменьшается. То есть вещество можно адсорбировать при невысокой температуре и десорбировать при более высокой.
Абсорбционное равновесие подвижно и может быть смещено в ту или иную сторону в соответствии с принципом Ле Шателье.
Количественно адсорбцию можно выражать в молях адсорбата на единицу площади адсорбента, моль/м2. Адсорбция зависит от природы адсорбента и адсорбата, температуры и концентрации или давления адсорбата. Кривую зависимости величины адсорбции Г от равновесных концентраций С или давлений р адсорбата при постоянной температуре Т называют изотермой адсорбции:
Г = f(C) или Г = f(p) при Т = const.
Изотерма адсорбции на однородной поверхности адсорбента была выведена американским ученым Дж.Лэнгмюром. При выводе уравнения было сделано предположение, что поверхность адсорбента однородна и при максимальном заполнении образуется мономолекулярный слой. В этом случае уравнение имеет вид:
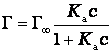
или
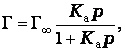
где Г∞ - адсорбция при максимальном заполнении;
с – равновесная концентрация адсорбата;
р – равновесное давление адсорбата;
Ка – константа равновесия процесса адсорбции.
 Графически
изотерма адсорбции имеет вид, приведенный на рис. 16
Графически
изотерма адсорбции имеет вид, приведенный на рис. 16
Изотерма Лэнгмюра редко соблюдается в реальности, поэтому предложены другие уравнения.
В 1906 г. Фрейндлих предложил эмпирическое уравнение изотермы. Уравнение Фрейндлиха имеет вид:
Г = Кфрn,
где Кф и n – постоянные.
5.4.4. Поверхностно-активные вещества
При адсорбции изменяются свойства поверхностного слоя, т.е. поверхностное натяжение. Адсорбирующиеся вещества могут понижать поверхностное натяжение (это поверхностно - активные вещества – ПАВ), повышать поверхностное натяжение (поверхностно - инактивные вещества) и не влиять на поверхностное натяжение (поверхностно - неактивные вещества).
Широкое применение нашли лишь ПАВ. Способностью уменьшать поверхностное натяжение, т.е. поверхностной активностью обладают молекулы вещества, имеющие неполярные гидрофобные углеводородные части ("хвосты") и полярные гидрофильные группы ("головы"). К полярным принадлежат группы
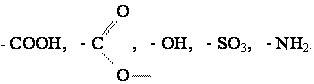
К ПАВ принадлежит натриевая соль стеариновой кислоты, входящей в состав мыла
СН3 ‑ (СН2)16 ‑ СООNa.
Поверхностная активность обусловлена гидрофобной частью молекул ПАВ ("хвостами"), которые выталкиваются из полярного растворителя, в то время как гидрофильные группы ("головы") удерживают молекулы ПАВ на границе раздела фаз. Таким образом, молекулы ПАВ адсорбируются на границе раздела фаз, причем гидрофобная их часть обращена в сторону газа или неполярной жидкости, гидрофильная часть – в сторону полярной жидкости или твердого гидрофильного адсорбента.
Концентрация ПАВ в поверхностном слое на несколько порядков выше, чем в объеме жидкости, поэтому даже при малом содержании ПАВ они значительно снижают поверхностное натяжение. Поверхностная активность ПАВ возрастает с увеличением длины углеводородной части молекул и их концентрации.
Изменение поверхностного натяжения под действием ПАВ влияет на смачиваемость твердых тел жидкостью. Этот эффект используется для очистки тканей (стирка, чистка) или металлов от жировых загрязнений применением ПАВ, при адсорбции которых на границе раздела фаз вода – жир, вода – твердое тело изменяется поверхностное натяжение воды на этих границах, что приводит к переходу жира в виде капель в водную среду.
Применение ПАВ позволяет разделять пустую породу и руду при флотации руд. Пустая порода смачивается водой, содержащей ПАВ, а руда поднимается вверх с пузырьками воздуха, продуваемого через раздробленную породу в воде.